

2025年7月10日,由沈琳教授团队牵头在国际权威学术期刊《自然-医学》(Nature Medicine)在线发表题为“A bispecific antibody–drug conjugate targeting EGFR and HER3 in metastatic esophageal squamous cell carcinoma: a phase 1b trial”研究成果。该研究首次全面报道了我国首创EGFR×HER3双抗ADC(BL-B01D1)药物在Ib期研究中晚期食管鳞癌患者的有效性和安全性,对于食管鳞癌靶向治疗具有突破性意义!

研究背景
伴随免疫治疗的快速发展,晚期食管癌鳞癌一线治疗以铂类化疗联合免疫治疗为主要治疗手段,然而多数患者都在面临棘手的耐药性问题。而对于免疫治疗耐药,二线治疗更是长期缺乏有效的治疗选择,整体获益不超过10%。因此,迫切需要开发新的、有效的治疗策略来克服当前疗法的局限性,提高食管鳞癌患者的生存率。
食管鳞癌普遍存在EGFR过表达,且与肿瘤侵袭性和较差的预后相关,然而既往的抗EGFR治疗(例如西妥昔单抗、帕尼单抗、吉非替尼等)研究并未对食管鳞癌展现出强有力的获益。最新研究表明,EGFR和HER3在消化道肿瘤中存在共表达,且与肿瘤发生和进展相关。临床前研究发现,同时靶向EGFR和HER3能达到更好的肿瘤杀伤效果,也因此成为新的潜在治疗方向。
BL-B01D1是我国首创靶向EGFR×HER3的双抗ADC药物,在结构上融合了EGFR和HER3双特异性抗体、基于四肽的可裂解连接子以及高效拓扑异构酶I抑制剂(Ed-04),其药物抗体比可达8,具有显著的抗肿瘤效果。BL-B01D1已被证实在肺癌、鼻咽癌、尿路上皮癌等多瘤种中具有不错的应用前景。考虑到晚期食管鳞癌患者常伴随营养不良、治疗耐受度差等安全性风险,本研究进一步评估了BL-B01D1在晚期食管鳞癌患者的有效性和安全性。
研究设计
本研究是一项全国多中心、开放标签、Ib期研究。研究人群是标准治疗失败的晚期食管鳞癌。设立了2.0mg/kg和2.5mg/kg共2个剂量组,分别在D1和D8给药,每3周为一个治疗周期。研究的主要终点是2期推荐剂量(RP2D),次要终点包括安全性、有效性、药代动力学和抗药抗体。探索性终点包括生存数据和疗效标志物探索。
研究结果
从2022年12月12日至2023年12月4日,共纳入82例晚期食管鳞癌患者接受BL-B01D1治疗,其中2.0mg/kg组22例,2.5mg/kg组60例。62.2%患者既往接受过2线及以上治疗,95.1%患者对于既往免疫治疗已耐药。数据截止2024年9月30日,仍有11例患者在组继续用药。
安全性方面,在2.5mg/kg组,最常见的不良反应包括贫血(85.0%)、血小板减少(58.3%)、白细胞减少(56.7%)以及中性粒细胞减少和恶心(均为46.7%)。在≥3级TRAE中,最常见的是贫血(28.3%),其次是白细胞减少和血小板减少(均为18.3%)和中性粒细胞减少(16.7%)。在2.0mg/kg组,最常见的不良反应为贫血(86.4%)、白细胞减少和乏力(均为45.5%)、血小板减少(40.9%)以及中性粒细胞减少和恶心(均为31.8%)。在≥3 级TRAE中,最常见的是贫血(27.3%)、淋巴细胞计数减少(13.6%)以及白细胞减少和中性粒细胞减少(均为9.1%)。
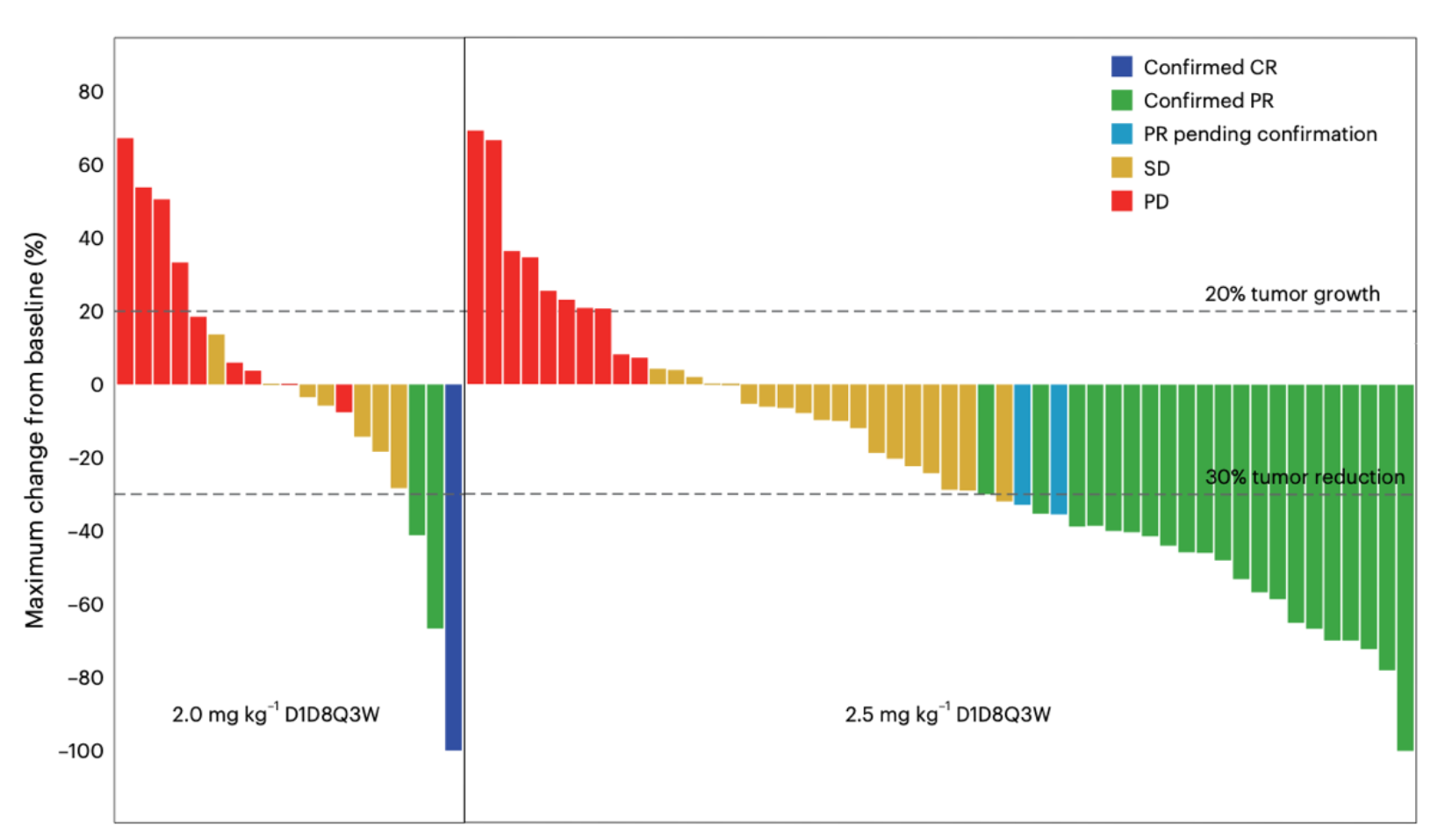
疗效方面,共73例患者具有可评估疗效,整体ORR 32.9%。2.5mg/kg剂量组和2.0mg/kg剂量组的疗效对比,ORR 39.6% vs. 15.0%,DCR 79.2% vs. 50.0%,中位PFS 5.4个月 vs. 2.7个月,中位OS 11.5个月 vs. 5.6个月。
综合比较2.5mg/kg和2.0mg/kg,两剂量组不良反应均可控,但2.5mg/kg疗效相对更优。因此最终选择2.5mg/kg D1D8 q3w作为食管鳞癌患者的RP2D。
研究结论
BL-B01D1在晚期食管鳞癌患者,尤其是既往免疫治疗失败的患者中表现出可控的安全性和令人鼓舞的抗肿瘤活性,实现了晚期食管癌鳞癌靶向治疗新突破。目前由沈琳教授牵头的BL-B01D1在晚期食管鳞癌二线的3期随机对照研究BL-B01D1-305研究(NCT06304974)正在全国多中心进行广泛开展,我们期待更进一步的循证医学结果,为更多晚期食管鳞癌患者带来福音。
本研究由北京大学肿瘤医院沈琳教授团队牵头,全国7家中心共同参与。鲁智豪教授、沈琳教授、龚继芳教授为通讯作者。北京大学肿瘤医院刘畅博士、刘丹博士、新乡医学院第一附属医院姬颖华教授为论文共同第一作者。
参考文献:Liu C, Liu D, Ji YH, et al.A bispecific antibody–drug conjugate targeting EGFR and HER3 in metastatic esophageal squamous cell carcinoma: a phase 1b trial. Nature Medicine 2025; DOI:10.1038/s41591-025-03792-7.
通讯作者:

鲁智豪,北京大学肿瘤医院消化肿瘤内科主任医师、教授、博士生导师。2008年毕业于北京大学,获肿瘤学博士学位,2014-2017年于美国Johns Hopkins医院从事博士后研究。长期从事食管癌的临床和转化研究。近年来共发表学术成果126篇,其中通讯作者/第一作者(含共同)40篇,包括:Nature、BMJ、Nature Medicine、J Clin Oncol等。单篇论文最高引用320次,2篇论文入选科睿唯安“高被引论文”。荣获中国抗癌协会青年科学家奖和中华医学科技奖一等奖等多项奖项。主持国家和省部级基金项目11项。入选国家第六批“万人计划”青年拔尖人才和北京市医院管理中心“登峰”人才培养计划(食管癌专业)。多项研究成果改写国内外肿瘤诊疗指南,获得北京大学博雅青年学者和中国抗癌协会青年科学家奖等。

沈琳,主任医师、教授、博士生导师,北京学者,北京大学肿瘤医院消化肿瘤内科主任、I期临床病区主任,实体瘤细胞与基因治疗北京市重点实验室主任。长期从事消化道肿瘤精准治疗与转化研究,以及抗肿瘤新药临床研究。建立消化道肿瘤临床与转化研究创新体系;作为Leading PI,主导百余项国际国内临床研究,促进新药获批适应症16项,成果改变国内外临床实践指南40多项;以通讯作者/第一作者在 Nature、BMJ、JAMA、Lancet、Nature Medicine等权威期刊发表 SCI 论文250余篇,15篇入选ESI 1%高被引论文,1篇入选1‰热点论文;入选“全球高被引科学家”。撰写54部国际国内诊疗规范;获国家专利18项,实现科技成果转化金额达1260万。获中华医学科技奖一等奖、中国抗癌协会科技奖一等奖等多项奖项。

龚继芳,主任医师,北京大学肿瘤医院I期临床病区主任副主任。长期从事抗肿瘤新药的早期临床研究和消化道肿瘤的内科治疗。近年来共发表学术成果50余篇,其中通讯作者/第一作者(含共同)在Nature Medicine等权威期刊发表。担任CSCO临床研究专业委员会委员兼秘书、中国抗癌协会抗癌药物专业委员会委员、中国药学会抗肿瘤专业委员会委员。