

基因治疗为重大疾病的治愈带来了新的机遇,然而基因治疗在临床上的应用很大程度上依赖于高效与安全的递送载体。本研究通过病毒包膜蛋白密码子定点突变技术和生物正交技术,通过基因重组和化学重组,构建了一种新的重组病毒样纳米粒。该制剂表现为显著降低的病毒样免疫原性,显著延长的血液循环时间和显著增强的弱酸病灶基因递送效率,携载基因编辑系统对乳腺癌荷瘤鼠具有显著基因编辑治疗效应,携载基因沉默系统对关节炎病理小鼠具有显著基因沉默治疗效果。本研究发展的重组病毒样纳米粒,有望作为高效、安全、靶向递送基因药物载体用于重大疾病的基因治疗,研究具有重要的科学意义和潜在的临床转化价值。
Bioorthogonal engineered virus-like nanoparticles for efficient gene therapy
Chun-Jie Bao1,2,3†, Jia-Lun Duan1,2†, Ying Xie1†, Xin-Ping Feng4, Wei Cui4, Song-Yue Chen1, Pei-Shan Li1, Yi-Xuan Liu1, Jin-Ling Wang1, Gui-Ling Wang1, Wan-Liang Lu1*
Nano-Micro Letters 2023, 15, 197
https://doi.org/10.1007/s40820-023-01153-y
本文亮点
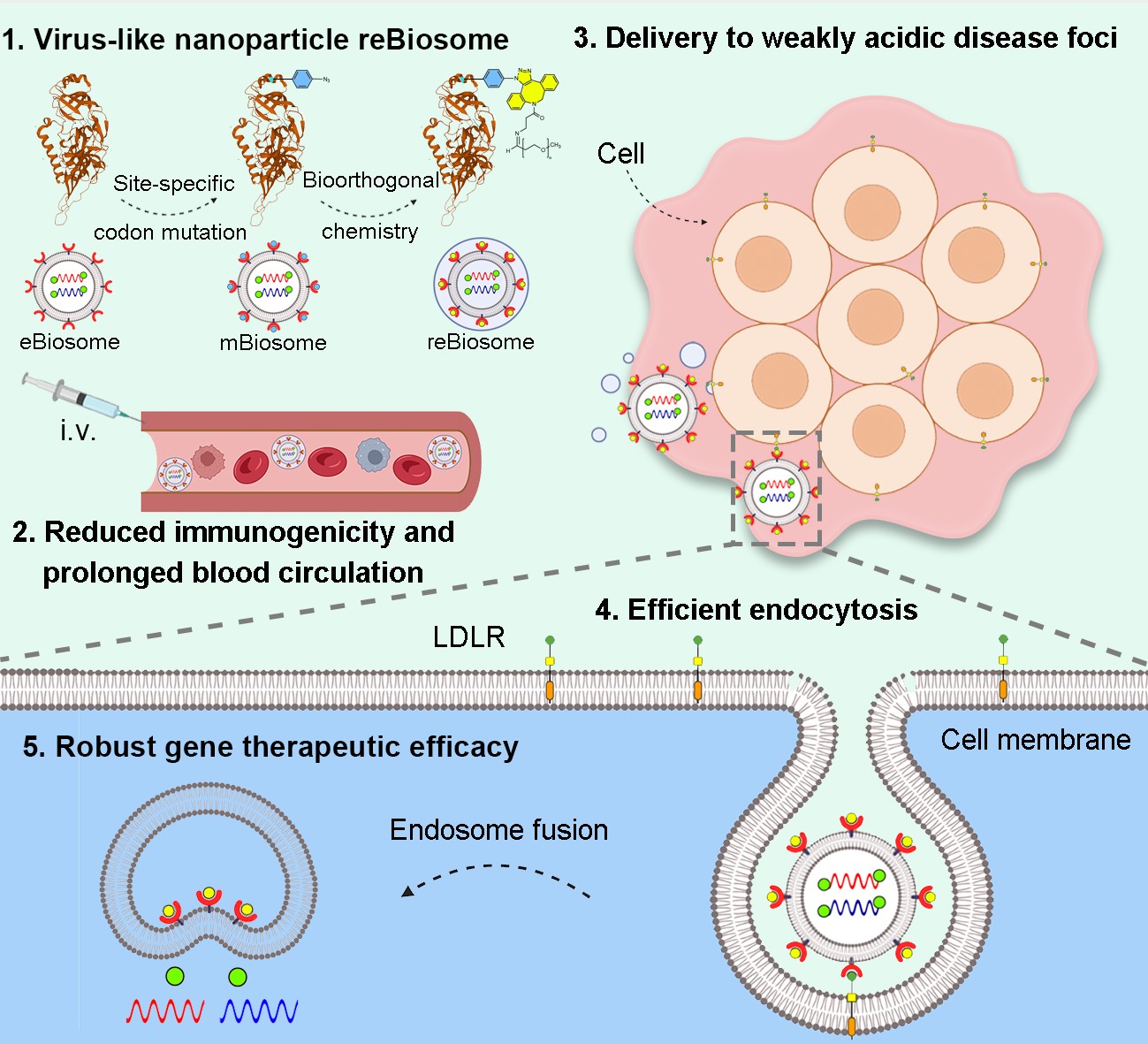
1. 研究通过密码子定点突变技术在病毒包膜蛋白的合理位点展示非天然氨基酸,继而通过生物正交化学技术将酸敏型材料偶联到非天然氨基酸,构建了一种新型重组病毒样纳米粒。
2. 研究发现,重组病毒样纳米粒在体内表现为显著降低的病毒样免疫原性,显著延长的血液循环时间和显著增强的弱酸病灶基因递送效率。
3. 研究将重组病毒样纳米粒用于基因编辑和基因沉默系统的递送,分别在乳腺癌和类风湿性关节炎的基因治疗中实现了显著的治疗效应。
内容简介
基因治疗为重大疾病的治愈带来了新的机遇,然而基因治疗在临床上的应用很大程度上依赖于高效与安全的递送载体。北京大学吕万良课题组首次报道了一种新型重组病毒样纳米粒(reBiosome)用于癌症和炎症性疾病的高效基因治疗。研究首先通过密码子定点突变技术在病毒样颗粒(eBiosome)的包膜蛋白上合理位点展示非天然氨基酸(Azi),得到定点突变病毒样颗粒(mBiosome)。继而,研究通过生物正交化学技术将弱酸性亲水聚合物偶联到mBiosome表面,从而制备得到reBiosome。结果表明,reBiosome在体内表现为显著降低的病毒样免疫原性,显著延长的血液循环时间和显著增强的弱酸病灶基因递送效率。研究将reBiosome分别用于基因编辑和基因沉默系统的递送,在乳腺癌和类风湿性关节炎的基因治疗中分别实现了显著的治疗效应。
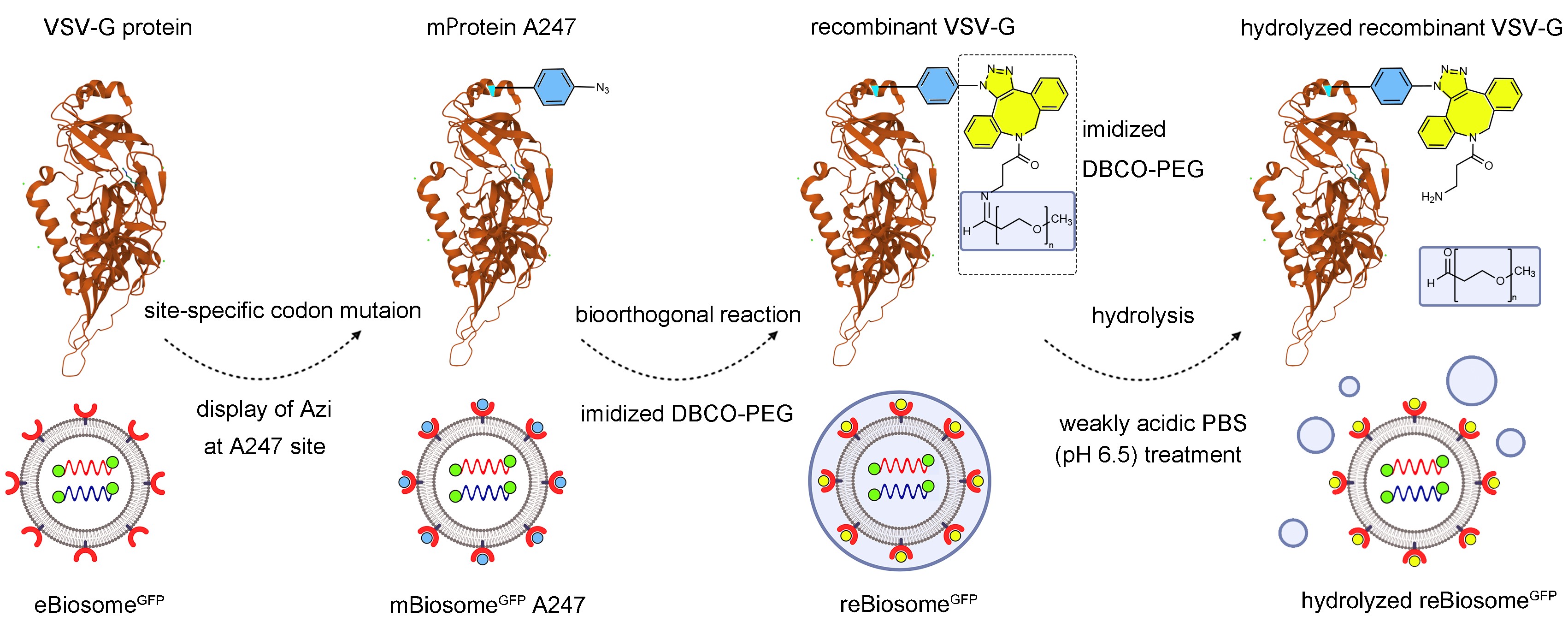
图1. reBiosome的制备路线及其酸敏感效应。第一步,通过密码子定点突变技术在病毒样纳米粒(eBiosome)的包膜蛋白VSV-G上合理位点展示非天然氨基酸(Azi),得到定点突变病毒样纳米粒(mBiosome)。第二步,通过生物正交化学技术将弱酸性亲水聚合物偶联到mBiosome表面,从而制备得到reBiosome。在弱酸处理下,reBiosome表面的弱酸性亲水聚合物得到水解,从而裸露出包膜蛋白VSV-G。
图文导读
Ⅰ 密码子定点突变病毒样纳米粒的制备及其基因转染效率
包膜蛋白VSV-G与其受体LDLR的结合构象如图2a所示。我们选择了红色圆圈区域的D192,A246,以及A247位点引入定点突变。图2b验证了定点突变后VSV-G的表达情况。图2c为VSV-G定点突变病毒样颗粒(mBiosome)的制备示意图。图2d-f分别是mBiosome上VSV-G的表达情况,mBiosome电镜形态以及粒径数据。结合3组数据看,这三种mBiosome制备成功,且在形态与粒径上相似。图2g为mBiosome与受体LDLR的结合-解离曲线;图2h, i为mBiosome与受体LDLR在细胞水平上的共定位情况。结合3组数据,mBiosome A247与受体LDLR的结合力较其他两种突变体强,且结合速度较快。图2j-l通过分子动态模拟从分子层面讨论了以上实验结果发生的可能原因。结果表明,三种mBiosome中,mBiosome A247构象较稳定,且其与受体结合面的电荷增加。图2m, n为细胞水平的基因转染效率,结果证明mBiosome A247的基因转染效率较其他两种突变体高。综合以上数据,我们选择mBiosome A247用于后续的生物正交工程化。
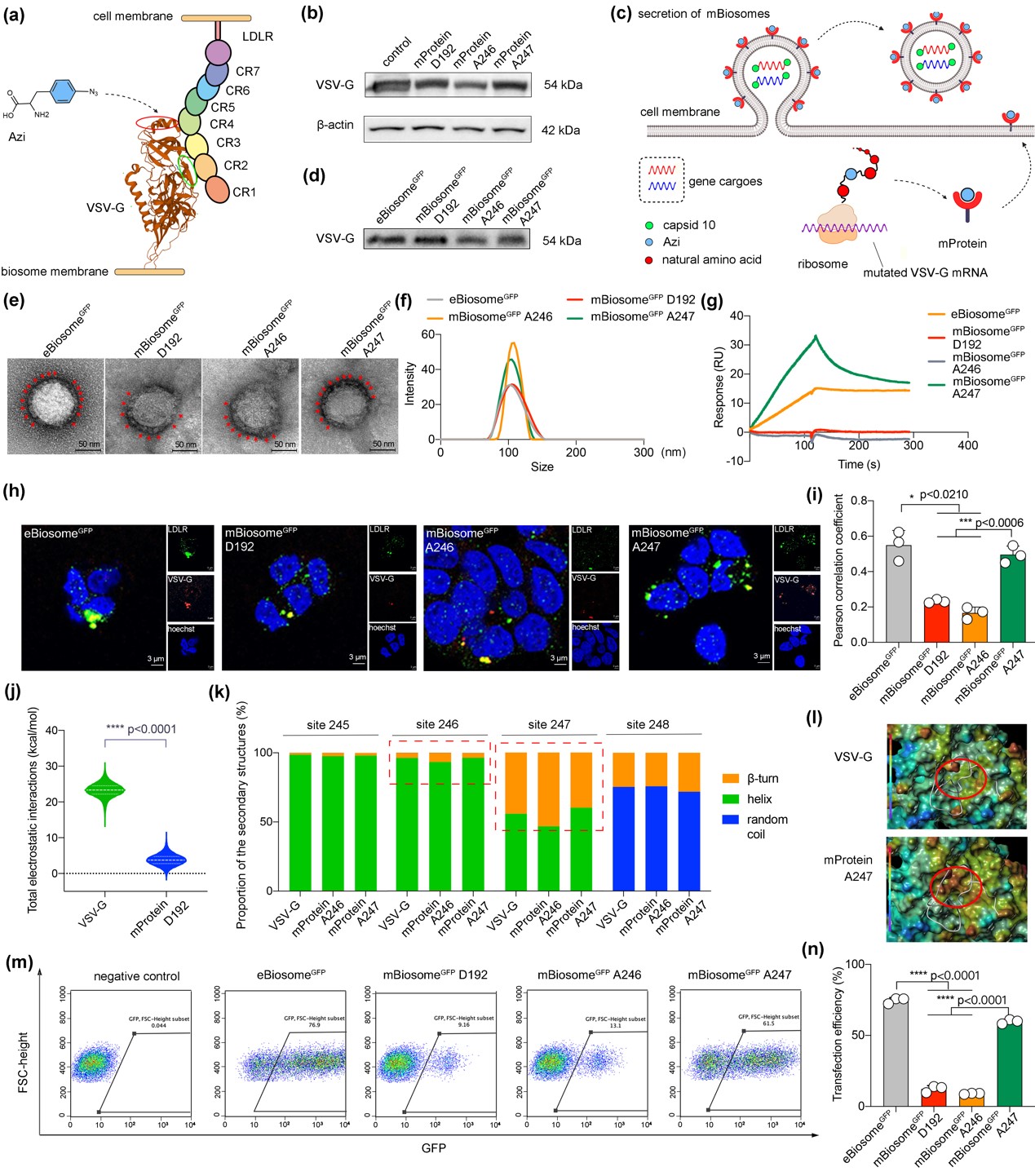
图2. 密码子定点突变病毒样纳米粒的制备及其基因转染效率。(a)密码子定点突变位点选择示意图;(b)定点突变后VSV-G的表达情况;(c)mBiosome制备示意图;(d)mBiosome上VSV-G的表达情况;(e)mBiosome电镜图;(f)粒径数据;(g)mBiosome与受体LDLR的结合-解离曲线;(h, i)mBiosome与受体LDLR在细胞水平上的共定位情况;(j-l)分子动态模拟结果;(m, n)细胞水平的基因转染效率。
Ⅱ 重组病毒样纳米粒的制备及其酸敏感效应
重组病毒样纳米粒(reBiosome)的制备路线及酸处理水解路线如上图1所示。图3a-b为reBiosome的电镜形态、粒径分布图。两组数据表明,reBiosome制备成功,且在酸处理后表面的聚合物部分被水解。图3c为reBiosome与受体LDLR的结合-解离曲线;图3d, e为reBiosome与受体LDLR在细胞水平上的共定位情况。结合3组数据,reBiosome与受体亲和力较低,酸处理后,其与受体亲和力显著提高。图3f,g为细胞对reBiosome的摄取效率。结果表明,细胞对reBiosome摄取效率极低,但对酸处理后的reBiosome摄取效率大幅提高。图3h,i为reBiosome在细胞水平上的基因转染效率。结合2组数据,reBiosome的基因转染效率较低,酸处理后,其基因转染效率显著提高。
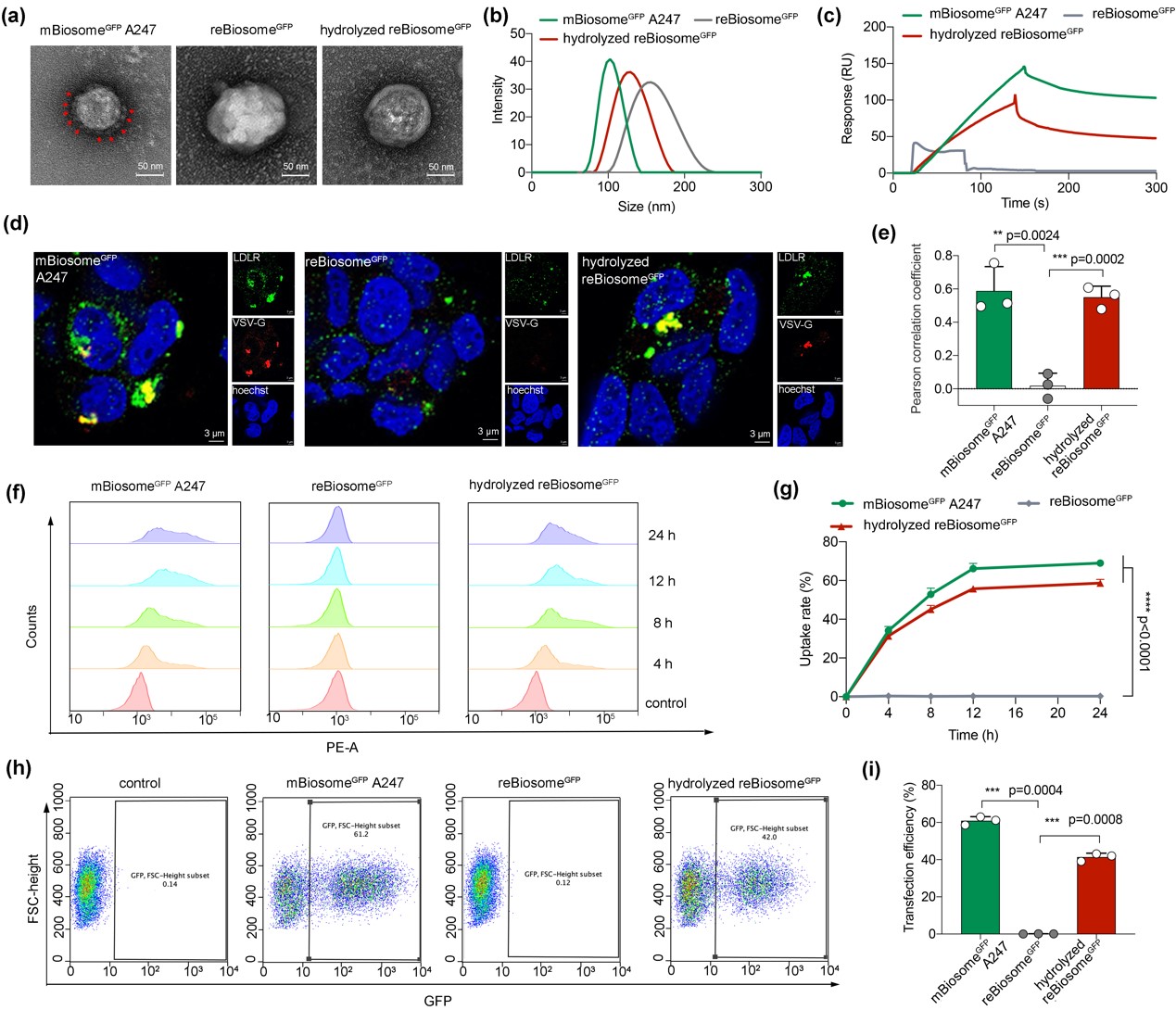
图3. 重组病毒样纳米粒的制备及其酸敏感效应。(a)电镜图;(b)粒径数据;(c)reBiosome与受体LDLR的结合-解离曲线;(d, e)reBiosome与受体LDLR在细胞水平上的共定位情况;(f)细胞对reBiosome的摄取效率;(h, i)细胞水平的基因转染效率。
III 重组病毒样纳米粒在体内的病毒样免疫原性降低,且血液循环时间延长
图4a为病毒样免疫原性检测指标示意图。图4b为血液中粒细胞(GR),单核细胞(MO)水平;图4c,d为血液中炎性细胞因子水平。结合3组数据,reBiosome处理组吞噬细胞水平(GR,MO)以及炎性细胞因子(CCL5,CXCL10,CCL2,CXCL1)水平较对照组病毒样纳米粒(eBiosome)处理组显著降低,表明reBiosome在体内的病毒样免疫原性显著低于eBiosome。图4e,f为不同时间点血液中病毒样纳米粒浓度。结合两组数据,reBiosome的体内循环时间显著比eBiosome长。
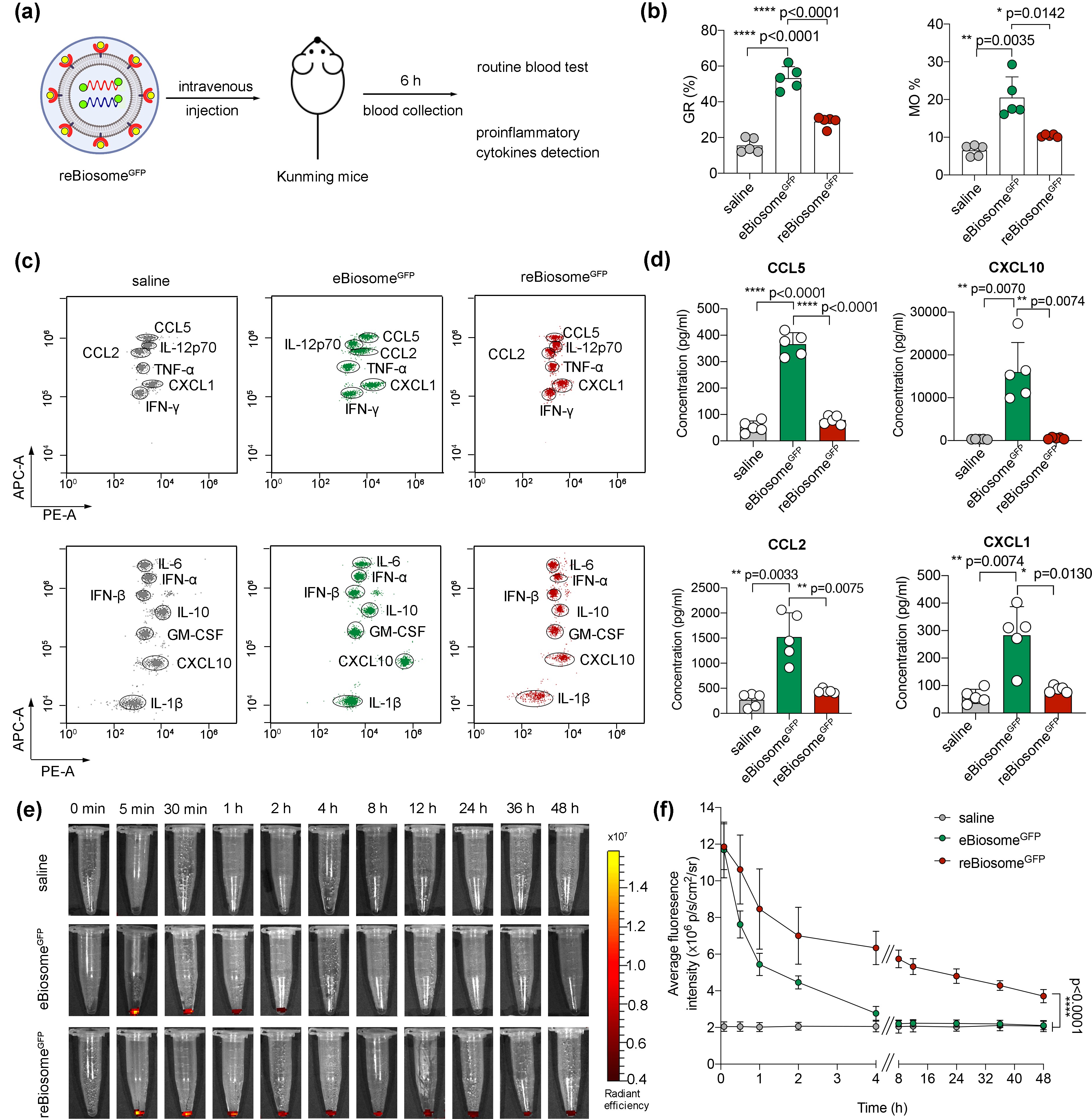
图4. 重组病毒样纳米粒在体内的病毒样免疫原性降低,且血液循环时间延长。(a)病毒样免疫原性检测指标示意图;(b)血液中吞噬细胞水平(GR,MO)水平;(c, d)血液中炎性细胞因子水平;(e, f)病毒样纳米粒药动学研究。
IV 重组病毒样纳米粒具有增强的弱酸病灶基因递送效率
图5a,b为DiR探针标记病毒样纳米粒在荷瘤小鼠肿瘤组织中的分布;图5c,d为DiR探针标记病毒样纳米粒在关节炎小鼠四肢中的分布;图5e,f为病毒样颗粒包封的GFP基因在荷瘤小鼠肿瘤组织中表达情况;图5g,h为病毒样颗粒携载的GFP基因在关节炎小鼠四肢中的表达情况。结合以上数据,与其他病毒样纳米粒相比,reBiosome在酸性病灶(肿瘤组织和关节炎组织)中具有增强的基因递送效率。
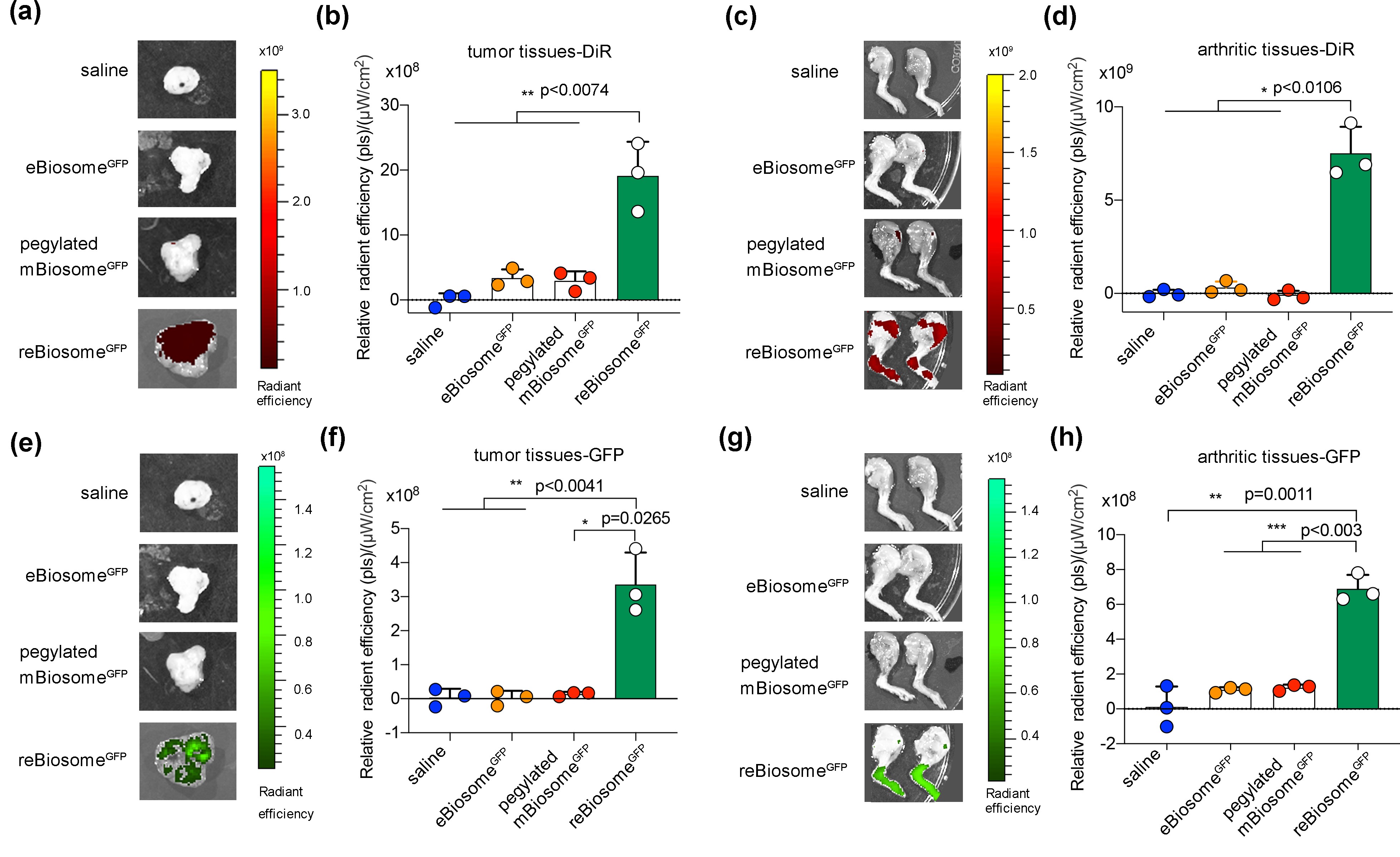
图5. 重组病毒样纳米粒具有增强的弱酸病灶基因递送效率。(a, b)肿瘤组织中病毒样纳米粒的分布;(c, d)关节炎组织中病毒样纳米粒的分布;(e, f)肿瘤组织中GFP基因的表达情况;(g, h)关节炎组织中GFP基因的表达情况。
V 载基因编辑系统重组病毒样纳米粒的抗乳腺癌效应
接下来,我们将reBiosome用于递送癌基因增强子αEmyc编辑系统,并研究其在体内抗乳腺癌效应,给药方案如图6a所示。其中αEmyc是本团队前期发现的癌基因c-Myc增强子,通过基因编辑手段敲除αEmyc可显著抑制乳腺癌细胞增殖。图6b,c为各处理组荷瘤小鼠肿瘤体积变化率;图6d为各处理组荷瘤小鼠在第16天的肿瘤组织重量。结合2组数据,载癌基因增强子编辑系统的重组病毒样纳米粒(reBiosomeaEmyc)可显著抑制肿瘤组织体积增长。图6e为肿瘤组织中c-Myc的表达情况,表明reBiosomeaEmyc可显著降低肿瘤组织中c-Myc的表达。图6f为肿瘤组织的苏木精-伊红(HE)染色结果;图6g,h为肿瘤组织中增殖抗原标志物ki67的表达情况;图6i,j为肿瘤组织细胞凋亡水平。结合3组数据,reBiosomeaEmyc可抑制肿瘤细胞增殖,促进肿瘤细胞凋亡。综合以上数据,reBiosomeaEmyc具有显著的抑制肿瘤生长的效应。
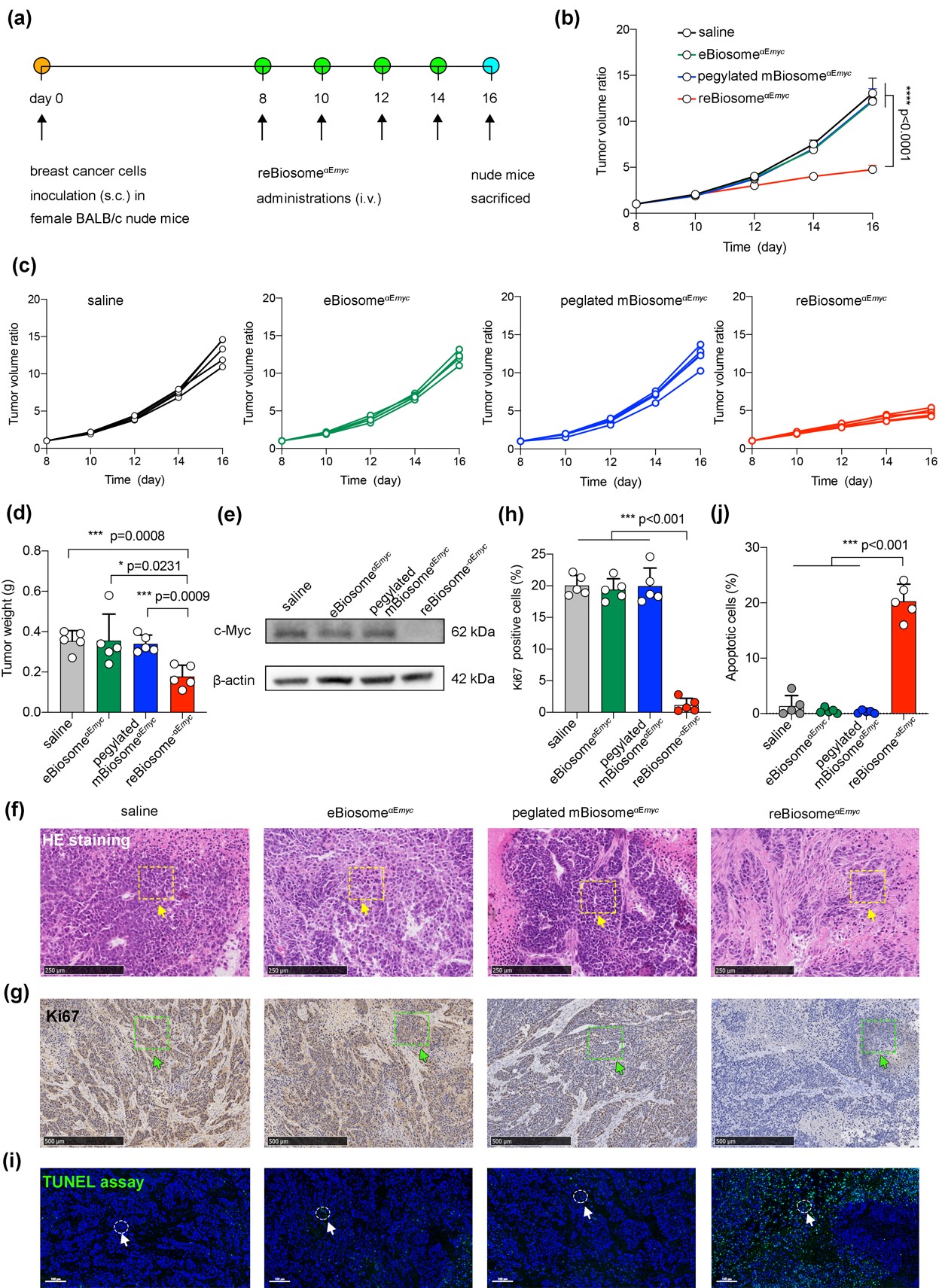
图6. 载基因编辑系统重组病毒样纳米粒的抗乳腺癌效应。(a)给药方案;(b, c)肿瘤体积变化率;(d)肿瘤组织重量;(e)肿瘤组织中c-Myc表达水平;(f)肿瘤组织HE染色结果;(g, h)肿瘤组织中增殖抗原标志物ki67的表达情况;(i, j)肿瘤组织细胞凋亡水平。
VI 载基因沉默系统重组病毒样纳米粒的抗类风湿性关节炎效应
最后,我们将reBiosome用于递送炎性细胞因子TNFα沉默系统,并研究其在体内抗类风湿性关节炎效应,给药方案如图7a所示。图7b,c为各处理组关节炎小鼠肿瘤关节炎评分变化,结果表明载基因沉默系统重组病毒样纳米粒(reBiosomeTNFα)可显著降低关节炎评分。图7d为各处理组小鼠跟骨的Micro-CT图像;图7e为小鼠膝关节组织的苏木精-伊红(HE)染色和番红-固绿(SF)结果。结合3组数据,reBiosomeTNFα可显著缓解关节炎对关节造成的骨损伤。图7f为血液中炎性因子TNFα的水平;图7g为膝关节中炎性因子TNFα的浸润情况。结合2组数据,reBiosomeTNFα可显著降低关节和血液中的TNFα水平。图7h为小鼠膝关节组织的抗炎巨噬细胞浸润情况,结果表明reBiosomeTNFα增加了关节中抗炎巨噬细胞的浸润。综合以上数据,reBiosomeTNFα具有显著的抗类风湿性关节炎效应。
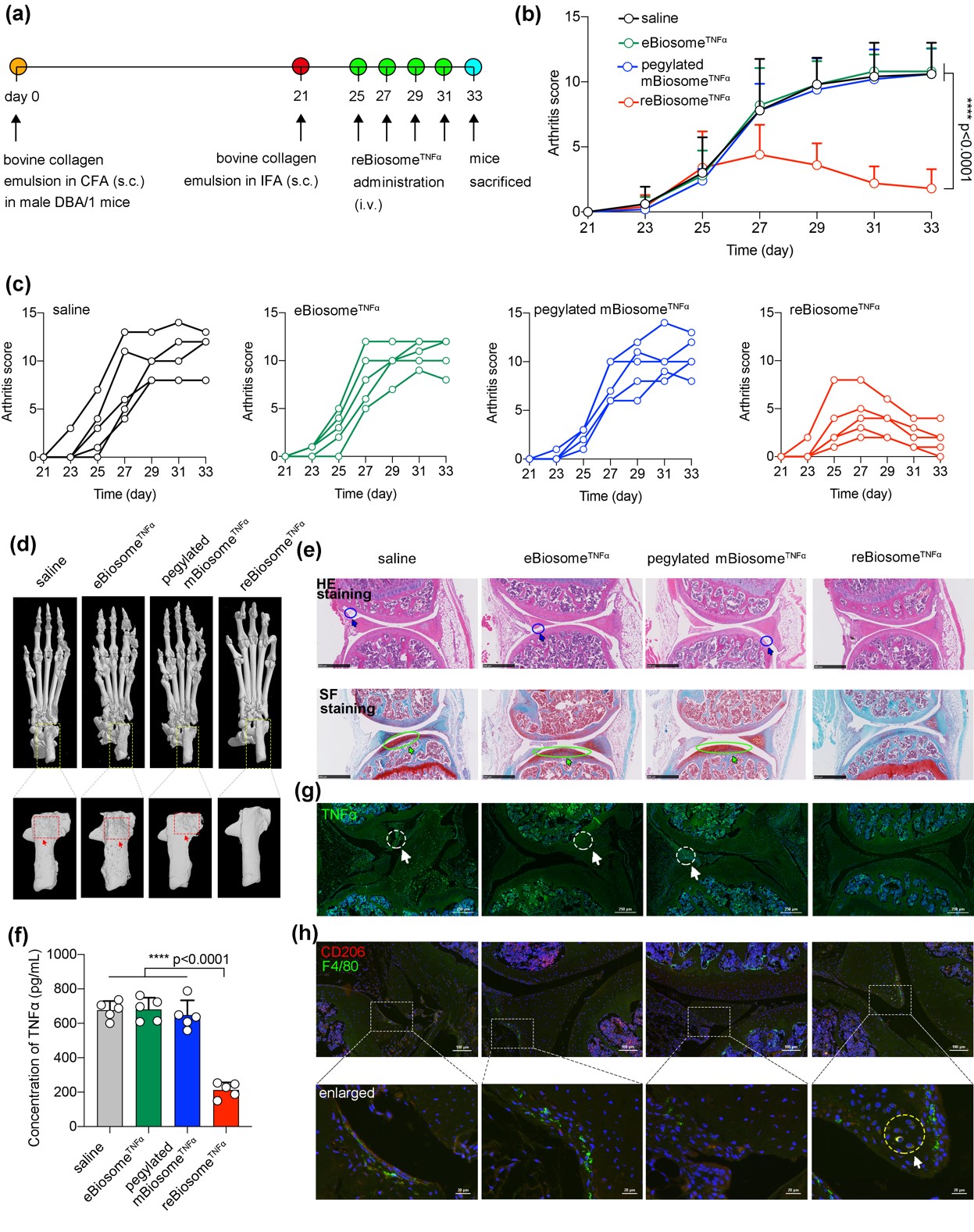
图7. 载基因沉默系统重组病毒样纳米粒的抗类风湿性关节炎效应。(a)给药方案;(b, c)关节炎评分变化;(d)跟骨关节Micro-CT成像;(e)膝关节组织HE染色及SF染色结果;(f)血液中TNFα水平;(g)膝关节中TNFα的浸润水平;(h)膝关节中抗炎巨噬细胞的浸润水平。
作者简介

包纯洁
本文共同第一作者
北京大学 博士/南京中医药大学 特聘教授(C类)
主要研究领域
生物药剂学与药物递送系统
个人简介
2023年毕业于北京大学药剂学专业,获得博士学位。2023年8月进入南京中医药大学担任医学院特聘教授(C类)。在《Nano-Micro Letters》、《Bioactive Materials》、《Chemical Engineering Journal》、《Molecular Therapy-Nucleic Acids》、《Clinical Translational Medicine》等国际高水平期刊发表SCI论文8篇,申请国家发明专利2项,致力于体内基因治疗用递送系统的开发。先后荣获国家奖学金、北京大学校长奖学金、北京市普通高等学校优秀毕业生等荣誉。

段嘉伦
本文共同第一作者
北京大学 博士/南京中医药大学 专任教师
主要研究领域:
(1)生物药剂学与药物递送系统
(2)中药资源新价值发现和利用
个人简介
2022年毕业于北京大学药剂学专业,获得博士学位。2022年8月进入南京中医药大学担任药学院专任教师。在《Bioactive Materials》、《Nano-Micro Letters》、《Molecular Therapy-Nucleic Acids》、《Chemical Engineering Journal》等国际高水平期刊发表SCI论文12篇。主持江苏省中药资源产业化过程协同创新中心开放课题重点项目1项,江苏省自然科学基金青年项目1项,江苏省高校自然科学研究项目面上项目(A类资助)1项,申请国家发明专利2项。先后荣获第二批全国高校“百名研究生党员标兵”、北京市优秀学生干部、北京大学优秀毕业生等荣誉。

谢英
本文共同第一作者
北京大学 副教授
主要研究领域:
新型药物递送系统与生物药剂学
个人简介
北京大学药学院副教授,硕士生导师,主持或作为共同申请人负责国家自然科学基金资助项目3项,作为主要研究人员参加国家重大科学研究计划(973)《纳米技术改善难溶性药物功效的应用基础》和重大新药创制:新制剂与新释药系统技术平台的研究工作。发表SCI论文30余篇,申请/授权专利10/4项。担任《Journal of Chinese Pharmaceutical Sciences》、《International Journal of Pharmaceutics》、《J Microencapsulation》、《Colloid and Surface, B》、《北京大学学报医学版》等学术期刊的审稿人。

吕万良
本文通讯作者
北京大学 长聘教授
主要研究领域
肿瘤干细胞、肿瘤耐药性与生物药剂学
个人简介
北京大学药学院长聘教授、博士生导师、分子药剂学与新释药系统北京市重点实验室副主任、天然药物及仿生药物国家重点实验室课题组长。学术兼任中国药学会药剂专业委员会主任委员、中国颗粒学会常务理事、北京大学学报(医学版)等期刊编委。发表论文180余篇,获2009、2012年度教育部自然科学一等奖、2019年度教育部自然科学二等奖等奖项。
(药学院)