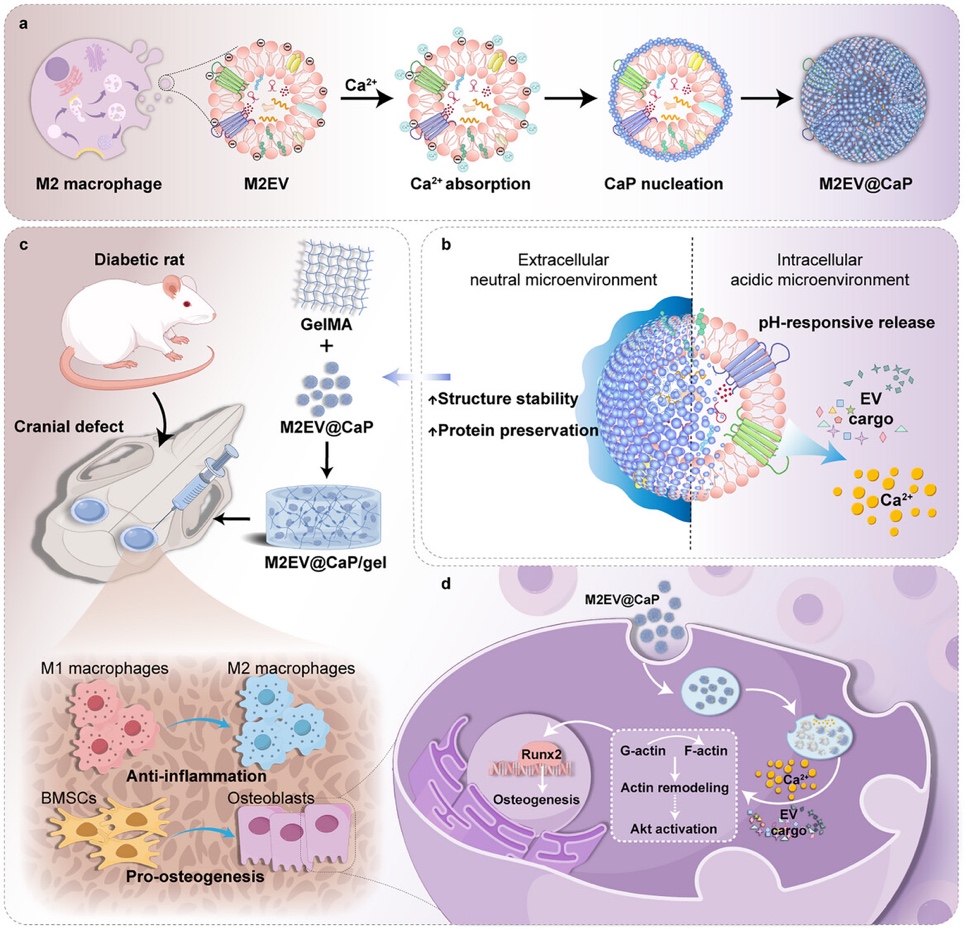
近日,由北京大学口腔医院、临床医学高等研究院、细胞稳态与衰老性重大疾病北京研究中心刘燕教授、王存玉院士团队、中科院北京纳米能源与系统研究所罗聃研究员团队与华中科技大学龚士强副教授团队合作的研究成果发表在《Advanced Materials》杂志上,标题为Calcium Phosphate Nanoparticle-Immobilized Macrophage-Derived Extracellular Vesicle Nanohybrid Facilitates Diabetic Bone Regeneration。研究团队以仿生矿化为灵感,在M2型巨噬细胞来源细胞外囊泡(M2EVs)表面原位生长无定形磷酸钙(CaP)纳米颗粒,构建“矿化披甲”的纳米杂化体(M2EV@CaP),实现对高糖炎性微环境的免疫重塑与成骨诱导双重调控,在糖尿病颅骨缺损模型中显著促进骨再生。

研究背景
糖尿病是全球性健康挑战,其导致的骨缺损修复障碍严重影响患者生活质量。慢性高血糖引发的持续性炎症损伤成骨功能,传统治疗手段因无法调控炎症微环境而效果欠佳。M2EVs凭借免疫调节和促分化特性在组织再生领域展现出广阔应用前景。然而,其临床转化面临两大核心挑战:一是结构稳定性差,在储存和递送过程中易发生聚集、降解和快速清除;二是成骨诱导能力不足,缺乏钙磷离子供给,无法有效启动生物矿化。现有细胞外囊泡稳定化策略存在操作复杂、结构损伤或免疫原性等问题,限制了临床应用。
由此,利用仿生矿化技术开发细胞外囊泡功能化策略以增强其稳定性和成骨诱导能力,实现复杂骨缺损模型的有效治疗,具有重要的科学意义和临床应用价值。
创新亮点
亮点一:仿生矿化“披甲”,显著提升囊泡稳定性与酸性响应释放
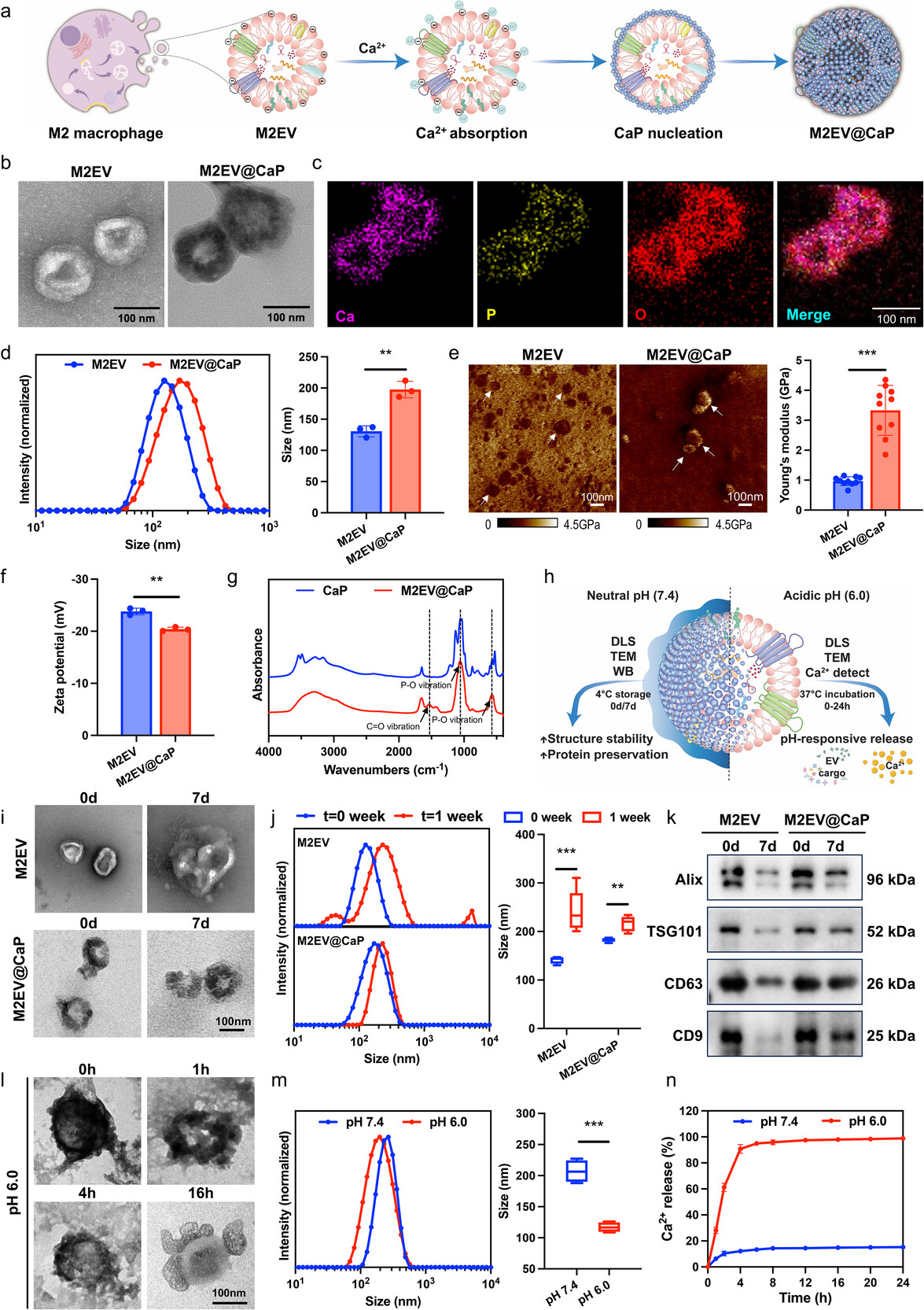
本研究借鉴生物矿化过程,在M2型巨噬细胞来源的细胞外囊泡表面实现磷酸钙纳米颗粒的原位生长,形成由无定形磷酸钙构成的有机—无机杂化外层。该矿化层在中性条件下作为良好稳定性的物理屏障,有助于在储存与递送环节维持囊泡结构与膜蛋白环境,降低聚集与成分失稳的发生。同时,磷酸钙外层作为可用钙/磷来源,在微酸性条件下发生可控降解,释放囊泡货载与离子,精准匹配骨修复的实际需求。通过稳定化包覆结合酸性触发释放设计,细胞外囊泡在复杂条件下的结构稳定性与递送有效性得到同步提升,确保了M2EV@CaP生物活性的有效发挥。
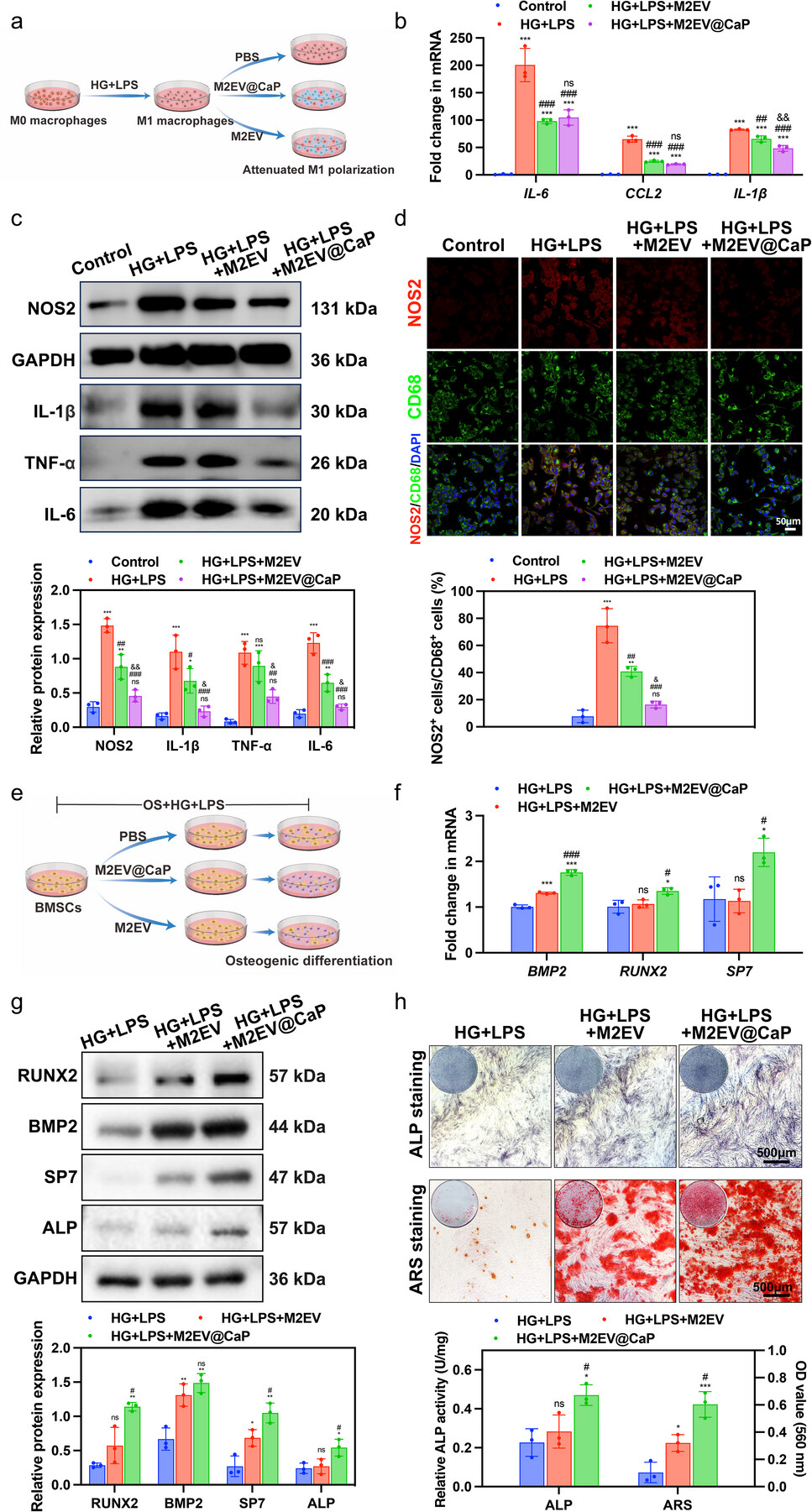
亮点二:免疫调控与成骨信号双驱动,促进高糖炎症微环境下干细胞成骨分化
M2EV@CaP展现出兼具免疫调控与成骨诱导的双重功能。在模拟糖尿病条件的高糖炎症环境中,M2EV@CaP显著抑制巨噬细胞M1型极化,下调促炎细胞因子的表达,有效改善炎症微环境。同时,M2EV@CaP显著增强骨髓间充质干细胞(BMSCs)的成骨分化能力。离子释放提升BMSCs胞内游离钙水平,诱导肌动蛋白细胞骨架重塑与整合素α5上调,进而激活PI3K/Akt通路并促进成骨转录因子表达。总的来说,通过“囊泡生物分子+矿物信号”的协同作用,M2EV@CaP在高糖炎症背景下同时作用于巨噬细胞与干细胞两个关键环节,为糖尿病相关骨再生提供了机制明晰、可实施的材料路径。
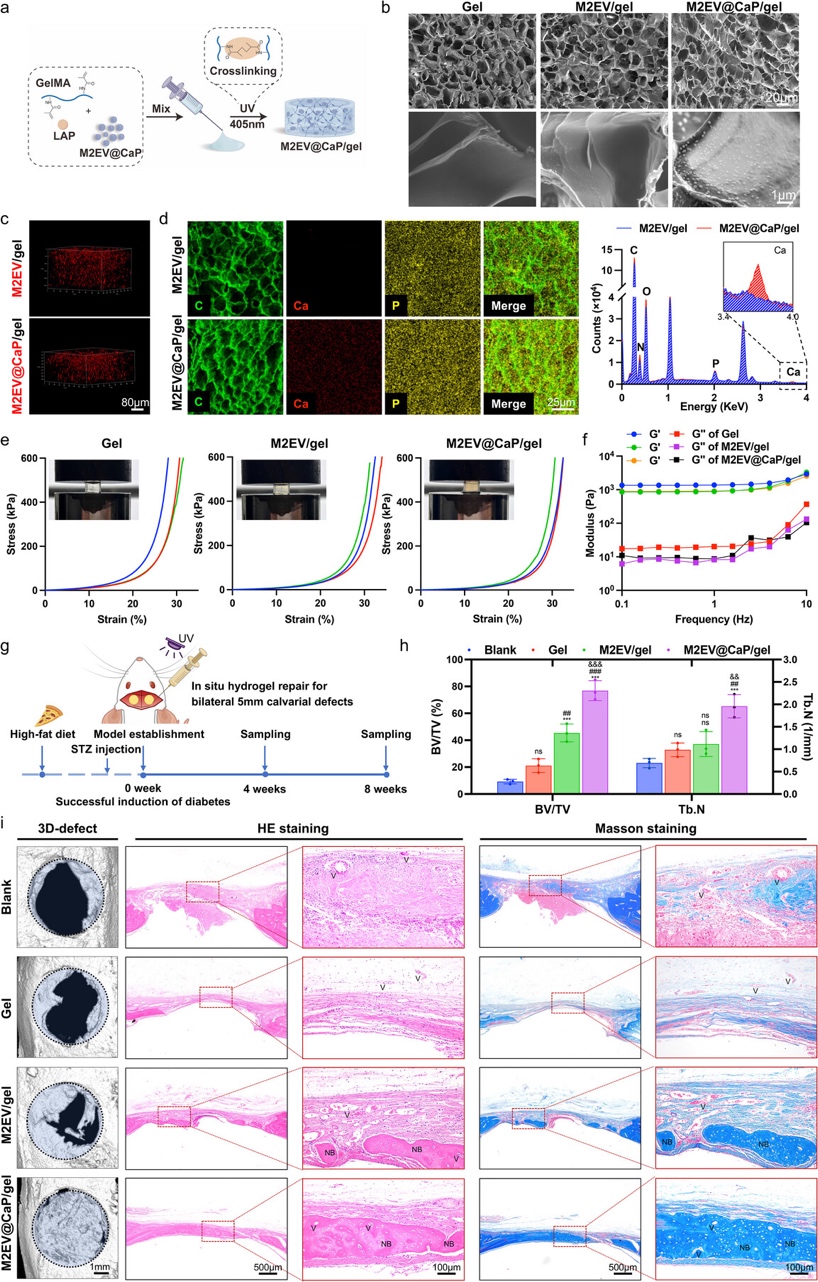
亮点三:水凝胶介导缓释递送与微环境重塑,实现糖尿病骨缺损高质量修复
在临床转化层面,研究团队将M2EV@CaP整合到明胶甲基丙烯酰(GelMA)水凝胶中,形成M2EV@CaP/gel复合递送系统。多孔基质为细胞浸润与营养交换提供通道,水凝胶网络限制囊泡过快扩散,磷酸钙纳米颗粒则在轻度酸性环境中触发离子与囊泡货载的顺序释放,增强局部信号的时空可控性。在糖尿病大鼠颅骨缺损模型中,M2EV@CaP/gel展现出优异的骨再生效果。免疫调控和成骨诱导的协同作用机制,使M2EV@CaP/gel有效打破糖尿病骨缺损中“炎症-修复抑制”的恶性循环,实现高质量骨再生,为糖尿病等复杂病理条件下的骨组织工程提供一种可行策略。
北京大学口腔医院、临床医学高等研究院、细胞稳态与衰老性重大疾病北京研究中心刘燕教授、王存玉院士、中科院北京纳米能源与系统研究所罗聃研究员、华中科技大学龚士强副教授为该论文共同通讯作者,北京大学博士吴晓岚为该论文第一作者。此外,该研究得到国家重点研发计划、国家自然科学基金重点项目等基金的经费支持。